LES FONCTIONS DES ZONES HUMIDES : Régulation des nutriments
| Les nutriments (Azote et Phosphore) sont des éléments nutritifs indispensables au développement des organismes autotrophes. Cependant, en excès, ces nutriments ont des effets néfastes sur les milieux aquatiques (eutrophisation,...). Les zones humides sont capables de retenir ces nutriments et participent ainsi à l’atteinte du bon état des masses d’eau (objectif de la DCE). |
I. QU’EST CE QUE LES NUTRIMENTS, LEURS ORIGINES ?
- L’azote
Formes de l’azote : L’azote est présent dans l’environnement sous forme réduite ou oxydée.
Les formes réduites de l’azote sont l’azote organique Norg (lié à un ou plusieurs atomes de carbone), apporté par les engrais et les détergents, et l’ammoniaque NH4+ issu de la dégradation de l’azote organique.
Les formes oxydées de l’azote (liées à un ou plusieurs atomes d’oxygène) sont les nitrites NO2- et les nitrates NO3-. Le nitrate est la forme de l’azote majoritaire dans l’environnement. Selon les conditions du milieu (concentration en oxygène, température, microorganismes,…) les nitrates peuvent subir différentes transformations chimiques. Les nitrites sont présents en faibles quantités dans l’environnement à cause de leur caractère instable.
Origine naturelle : L’azote est un constituant naturel de la croûte terrestre et entre dans la composition de certains minéraux (ex : nitrates de potassium KNO3).
Origine anthropique : L’azote entre dans la composition des engrais minéraux, très utilisés en agriculture pour favoriser la croissance des cultures. Les plantes prélèvent les nutriments du sol pour réaliser leur métabolisme. L’excédant entre ce qui est apporté par les engrais et ce qui est prélevé par la plante représente une menace pour l’environnement. Ainsi, l’azote peu soluble, peut être lessivé des sols et rejoindre les cours d’eau de surfaces ou s’infiltrer jusqu’à la nappe phréatique entrainant une pollution de ces eaux qui peut se traduire par une eutrophisation du milieu.
L’industrie produit de l’azote atmosphérique (ex : oxydes d’azote : NOx). Les dépôts atmosphériques qui en résultent sont potentiellement capables de polluer des zones humides très éloignées de la source de la pollution (cas de pollution sur des tourbières oligotrophes).
- Le phosphore
Formes du phosphore : le phosphate soluble est la forme oxydée la plus courante dans l'eau. On rencontre également les formes organiques plus ou moins mobiles ou assimilables.
Origine naturelle : le phosphore est présent dans l’environnement dans les roches phosphatées. La dissolution de ces roches par les précipitations entraine une dissolution du phosphore qui peut alors être lessivé jusque dans les cours d’eau.
Les apports naturels de phosphore dans les milieux aquatiques restent très faibles. Le phosphore est un facteur limitant de la croissance des végétaux.
Origine anthropique : La majorité du phosphore retrouvé dans les milieux aquatiques a une origine anthropique. En effet, celui-ci entre dans la composition des détergents (ex : lessives) et des engrais phosphatés. Lors de rejets d’eaux usées domestiques directement dans le milieu naturel, un enrichissement des eaux en phosphore est observé pouvant être à l’origine d’un phénomène d’eutrophisation.
II. ENJEUX LIES A LA REGULATION DES NUTRIMENTS
| L’eutrophisation correspond à un enrichissement de l’eau en éléments nutritifs, notamment des composés de l’azote et/ou du phosphore, provoquant un développement accéléré des algues et des végétaux qui entraîne une perturbation indésirable de l’équilibre des organismes présents dans l’eau et une dégradation de la qualité de l’eau (diminution des concentrations en oxygène, mortalité des organismes, développement de toxines,…). |
Outre le risque environnemental lié à une utilisation excessive de nutriments, le risque sanitaire est bien réel. La contamination d’une ressource d’eau potable ou d’une zone de baignade peut engendrer un risque pour la santé (cyanobactéries toxiques) et en particulier pour les personnes sensibles (personnes âgées, femmes enceintes, enfants,…).
Ainsi, une substance peut être bénéfique pour un environnement et délétère pour un autre (biodisponibilité du phosphore dans le sol agricole VS biodisponibilité du P dans les milieux aquatiques)
III. MECANISMES DE REGULATION DES NUTRIMENTS PAR LES ZONES HUMIDES
- régulation des nitrates
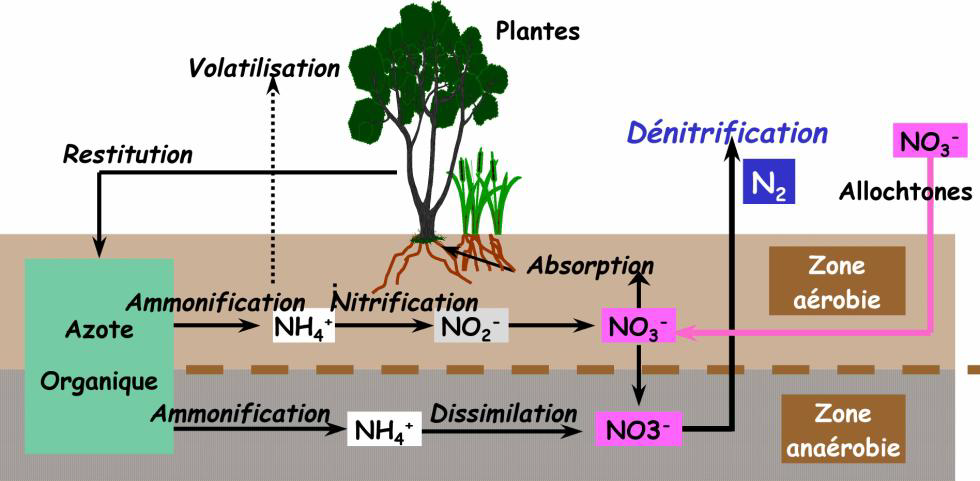
L’azote est présent sous différentes formes chimiques dans les eaux. Il peut être organique (c'est-à-dire fixé à un ou plusieurs atomes d’oxygène : nitrates, nitrites) ou minéral (ammoniaque). Différents mécanismes existent naturellement au sein des zones humides à l’origine d’une régulation de l’azote :
- interception/rétention : l’azote organique et les ions ammoniums associés à des particules sont captés par les végétaux et les microorganismes. L’azote est ensuite stocké par les végétaux. Le temps de stockage est variable en fonction des végétaux (espèces, stade de développement) : les espèces « annuelles » ne stockent l’azote que sur une période d’une année, celui-ci étant relargué à la mort de la plante. Certaines espèces vivaces sont donc à privilégier car elles effectuent un stockage à plus long terme.
- Ammonification/Minéralisation de l’azote organique par voie microbienne: cette réaction a lieu dans la partie non saturée du sol de la zone humide (partie supérieure du sol). La minéralisation correspond à la transformation de l’azote organique en ammoniaque (Norg NH4+) qui sera par la suite transformé en nitrites et en nitrates par la réaction de nitrification (NH4+ NO2- NO3-). Les nitrates solubles peuvent ensuite être assimilés et stockés par la plante ou s’infiltrer en profondeur où ils seront éliminés par dénitrification.
- Dénitrification par les microorganismes : ce processus a lieu dans la partie saturée du sol (absence d’oxygène dissous). Il est réalisé par les microorganismes hétérotrophes aérobies facultatifs qui utilisent soit l’oxygène moléculaire (O2) soit l’oxygène lié aux nitrates. En conditions anaérobies dans les sols (absence d’oxygène moléculaire) les microorganismes consomment l’oxygène lié aux nitrates. La réaction qui a lieu correspond à une réduction de l’azote trivalent (= nitrates liés à trois atomes d’oxygène NO3-) en azote divalent (=nitrites liés à deux atomes d’oxygène NO2-) puis en azote gazeux (NO3- (NO2-) N2) relargué dans l’atmosphère. Les nitrites étant instables, le passage de nitrites à azote gazeux se fait très rapidement, cette étape n’est donc pas représentée sur la figure 1.
Les conditions requises pour la réalisation de la dénitrification sont les suivantes : saturation en eau du sol + présence de microorganismes + présence de nitrates + matière organique biodégradable + température favorable à l’action microbienne. Dans ces conditions, la zone humide peut dénitrifier entre 40 et 150 kilos de nitrates par hectare de zone humide et par an (= entre 10 et 40 mg/m²/j soit pour une zone humide de 1 ha 1 à 4 kg N/j).
Les microorganismes étant sensibles aux conditions de température, la notion de région climatique est à prendre en compte dans la réalisation de la dénitrification. Ainsi, dans le cas des zones humides d’altitude ayant des températures plus faibles, la fonction épuratoire de l’azote est généralement moins importante.
L’efficacité de la fonction de rétention et d’élimination de l’azote par les zones humides est variable en fonction du type de zone humide. Dans le cas de zones humides quasi fermées, la rétention de l’azote et presque totale et dépend d’un certain nombre de facteurs comme la végétation, la biodégradabilité de la MO ou encore les conditions RedOx du milieu.
Pour les zones humides riveraines des cours d’eau, la surface de zone humide importe moins que son linéaire. La présence de ces zones humides est importante notamment en zone agricole, de par leur position à l’interface entre milieu terrestre et milieu aquatique. Elles jouent un rôle épuratoire au même titre que la bande enherbée et permet de réduire les quantités de nitrates arrivant jusqu’au cours d’eau (figure 2).
En milieux côtiers et estuariens, la fonction de régulation de l’azote est plus marquée dans les zones de basses eaux fréquemment immergées et dans les zones dépressionnaires des marais salés.
2. régulation du phosphore
Les différentes formes du phosphore (particulaire, dissous) subissent différents mécanismes qui aboutissent à la régulation des quantités de phosphore circulantes.
- Déposition du phosphore particulaire : Lors de la traversée de la zone humide, le ralentissement du courant est à l’origine d’un phénomène de sédimentation. Ce mécanisme est similaire au mécanisme de rétention des matières en suspension (MES).
- Immobilisation du phosphore dissous par précipitation avec le fer, le calcium ou l’aluminium. La précipitation entraîne une diminution des concentrations de phosphore en solution et la formation d’un solide. Ce mécanisme est à l’origine d’une immobilisation du phosphore. Dans certaines conditions, le phénomène inverse est observé. Il s’agit de la dissolution qui entraine une remise en solution du phosphore qui redevient mobile.
- Immobilisation du phosphore dissous par adsorption sur des argiles. L’adsorption est un phénomène de surface lors duquel le phosphore va se fixer sur des sites d’adsorption disponibles à la surface du sol. Les ions phosphates sont chargés négativement, ils seront donc principalement adsorbés par des sols présentant un pH acide (possédant des charges de surface majoritairement positives). La quantité de sites d’adsorption détermine la quantité de phosphore immobilisé par adsorption. De plus, il est possible d’observer un phénomène de compétition d’autres ions négatifs avec le phosphore pour l’occupation des sites d’adsorption du sol. L’adsorption est un phénomène réversible où selon les conditions du milieu le phosphore peut être adsorbé ou désorbé.
|
Les solides possèdent de nombreux groupes fonctionnels de surface et présentent une charge de surface qui leur confère d’importantes propriétés adsorbantes. Dans les sols, les principaux adsorbants sont la matière organique, les oxydes ou hydroxydes métalliques et les argiles. Les fonctions de surfaces sont généralement assimilées à des groupements hydroxyles de surface notés ≡ S-OH. Ces fonctions ionisables des sites de surface vont se comporter comme des substances amphotères (= elles peuvent être soit des bases soit des acides). Elles peuvent ainsi échanger des protons selon : (1) ≡ S-OH → ≡ S-O- + H+ (pH basiques) Pour les pH acides, la charge de surface sera positive. Les fonctions de surface se comportent comme des bases. Inversement, elle sera négative pour des pH basiques. Les fonctions de surface se comportant ici comme des acides. |
- Assimilation des ions phosphates (H2PO4-, HPO42-, PO4-) par les végétaux. Les ions phosphates sont assimilés par les végétaux pendant leur période de croissance. Une partie du P stocké reste durablement dans la plante au niveau des organes pérennes. Une autre partie retourne dans l’eau ou dans le sol lors de la mort de la plante ou de la chute des feuilles.
- Immobilisation d’une partie du phosphore soluble par la biomasse microbienne surtout dans certaines tourbières. Le développement de la biomasse microbienne implique l'absorption et l'immobilisation d'une partie du phosphore soluble. Ce processus peut être négligeable dans des milieux où la composante minérale est grande, mais important dans les sols organiques de certaines tourbières.
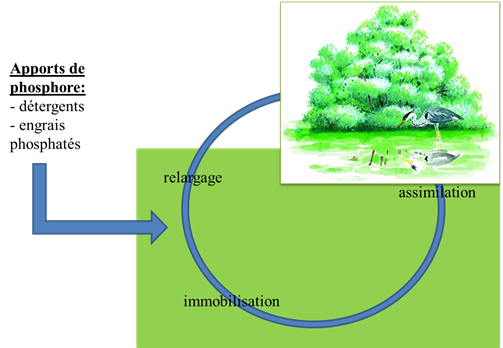
Selon le type de zone humide considéré, l’efficacité de la rétention du phosphore varie. Dans les zones humides fermées, le phosphore particulaire et dissous est stocké durablement dans la zone (figure 3). Celui-ci passe d’un compartiment à un autre selon les saisons.
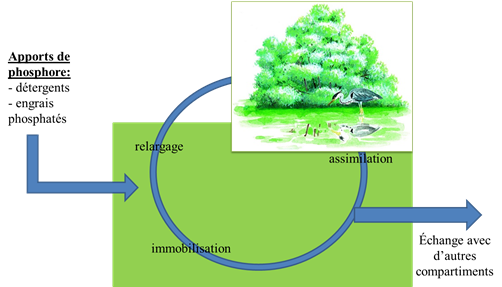
Dans les systèmes ouverts, le stockage du phosphore est variable. Il est immobilisé lors des crues hivernales puis prélevé par la végétation. A la mort de la plante, le phosphore retourne dans les eaux ou dans le sol. Le stockage du phosphore est variable selon l’intensité des échanges avec les autres milieux (figure 4).
Suivant le type de zone humide et le type de végétation associée, les mécanismes de régulation des nutriments sont différents. La végétation des zones humides joue un rôle majeur dans l’abattement du taux de nutriments.
Retenons par exemple que :
- Les plantes à rhizomes (plantes vivaces possédant des organes de réserve souterrains) constituent des pièges à nutriments efficaces : roseaux, phalaris, nénuphars, nassette).
- Les plantes annuelles absorbant les nutriments par leurs racines, immobilisent le phosphore pendant la durée de leur cycle de vie (une année) et le relarguent ensuite dans le milieu à leur mort. La rétention n’est donc que temporaire.
- Les espèces arbustives et arborescentes stockent durablement le phosphore dans les troncs et les branchages. Une faible partie du phosphore stocké retourne dans le milieu lors de la chute des feuilles.
A titre indicatif voici quelques ordres de grandeur mesurés pour la dénitrification.
| Type de milieux | Pertes d’azote | Références |
|---|---|---|
| Ripisylve (potentiel) | 340 mg N/m²/j | Pinay, 1986 |
| Ripisylve (potentiel) | 260 mg N/m²/j | Seitzinger, 1994 |
| Saulaie (potentiel) | 240 mg N/m²/j | Fustec, 1988 |
| Aulnaie (potentiel) | 130 mg N/m²/j | Fustec & al., 1991 |
| Prairie mal drainée | 30 mg N/m²/j | Schnabel & Stout 1994 |
| Prairie mieux drainée | 0,7 mg N/m²/j | Schnabel & Stout 1994 |
| Sédiments côtiers | 0,7 à 3,5 mg N/m²/j | Seitzinger, 1988 |
| Marais salé | 67,5 mg N/m²/j | Kaplan & al., 1979 |
| Marais salé (potentiel) | 25,2 mg N/m²/j | White & Howes, 1994 |
| Slikke | 3 mg N/m²/j | Valieda & Teal, 1979 |
| Marais à juncus | 4,3 mg N/m²/j | Reddy & al., 1989 |
| Estuaire | 1,2 mg N/m²/j | Jenkins & Kemps, 1984 |
| Tourbière acide | < 50 µg N/m²/j | Urban & al., 1988 |
| Lacs | 1 à 60 mg N/m²/j | Seitzinger, 1988 |
| Plans d’eau | 3,7 mg N/m²/j | Smith & De Laune, 1983 |
En résumé, le tableau suivant présente une évaluation qualitative du rôle des différents types de zones humides dans la fonction de régulation des nutriments.
| Type SDAGE | Sous type de ZH | Régulation nutriments | |
|---|---|---|---|
| 1 | Grands estuaires | ||
| 2 | Baies et estuaires moyens et plats | Baies et estuaires moyens et plats | |
| Vasières | |||
| 3 | Marais et lagunes côtiers | Marais et lagunes côtiers | |
| 4 | Marais saumâtres aménagés | Marais saumâtres aménagés | |
| 5 | Bordures et cours d’eau | Ripisylves | |
| Vasières | |||
| 6 | Plaines alluviales | Prairies alluviales | |
| Forêts alluviales | |||
| Bras morts et secondaires | |||
| Marais alluviaux | |||
| Grèves et bancs d’alluvions | |||
| Berges végétalisées | |||
| Berges nues | |||
| 7 | Zones humides de bas fonds en tête de bassin | Marais | |
| Prairies humides | |||
| Tourbières | |||
| Milieux fontinaux | |||
| Petites zones humides de fond de vallée | |||
| 8 | Régions d’étangs | Etangs (>1000m²) | |
| 9 | Bordures de plans d’eau | Bordures de plans d’eau | |
| 10 | Marais et landes humides de plaines et plateaux | Marais | |
| Prairies humides | |||
| 11 | Zones humides ponctuelles | Mares et étangs isolés | |
| 12 | Marais aménagés dans un but agricole | Marais cultivés, rizières | |
| 13 | Zones humides artificielles | Carrières réaménagées | |
| Bassins de décantation et autres |
| Absence de rôle avéré | Rôle important | Rôle moyen |
Limites de la fonction :
Il ne faut cependant pas considérer les zones humides comme des systèmes d’épuration. En effet, des rejets bruts non traités voire même une quantité incontrôlée de rejets traités peuvent engendrer une pollution de la zone humide.
Certaines actions comme le retournement des sols peuvent être à l’origine d’une remobilisation du phosphore et de l’azote contenu dans les sols des zones humides.
La fonction de régulation de l’azote est donc à privilégier dans le cas de dossiers concernant des zones humides soumises à de fortes pressions (anthropiques et agricoles). En effet, ces zones ont un rôle de protection de la qualité des cours d’eau à jouer.
Exemples tirés de doc RMC 2006 illustrant l’importance des zones humides dans la régulation des nutriments [3]:
- 60 à 95% du phosphore particulaire introduit dans les zones humides riveraines des petits cours d’eau à l’amont des bassins qui alimentent des lacs est immobilisé avant d’atteindre les eaux de surface (Peterjohn et Correll, 1984)
- En moins de 30 m une ripisylve peut abattre de 80% la teneur en nitrates du bassin versant (Lefeuvre, Colloque zones humides, oct. 1994)
- 60 à 95% de l’azote associé aux particules mises en suspension et transportées par les eaux de ruissellement sont piégés par les ripisylves en particulier dans les petits bassins versants en tête de réseaux hydrographique (Fustec et Frochot, 1994)
SYNTHESE :
Régulation des nutriments
Les nutriments (Azote et Phosphore) sont des éléments nutritifs indispensables au développement des organismes autotrophes. Cependant, en excès, ces nutriments ont des effets néfastes sur les milieux aquatiques (eutrophisation,...). Les zones humides sont capables de retenir ces nutriments et participent ainsi à l’atteinte du bon état des masses d’eau (objectif de la DCE).
La fonction de régulation de l’azote est donc à privilégier dans le cas de dossiers concernant des zones humides soumises à de fortes pressions (anthropiques et agricoles). En effet, ces zones ont un rôle de protection de la qualité des cours d’eau à jouer.
L’azote et le phosphore sont régulés au sein des zones humides par différents mécanismes :
| azote | phosphore | |
|---|---|---|
| Mécanismes de régulation |
|
|
Les mécanismes de régulation des nutriments mis en jeu sont variables suivant le type de zone humide et le type de végétation associée. La végétation des zones humides joue un rôle majeur dans l’abattement du taux de nutriments.
A titre d’exemple, 60 à 95% du phosphore particulaire introduit dans les zones humides riveraines des petits cours d’eau à l’amont des bassins qui alimentent des lacs est immobilisé avant d’atteindre les eaux de surface (Peterjohn et Correll, 1984). De plus, en moins de 30 mètres, une ripisylve peut abattre de 80% la teneur en nitrates du bassin versant (Lefeuvre, Colloque zones humides, oct. 1994)
Il ne faut cependant pas considérer les zones humides comme des systèmes d’épuration. En effet, des rejets bruts non traités voire même une quantité incontrôlée de rejets traités peuvent engendrer une pollution de la zone humide.
Certaines actions comme le retournement des sols peuvent être à l’origine d’une remobilisation du phosphore et de l’azote contenu dans les sols des zones humides.